Impact of the hERG Channel Mutation N588K on Electrical Properties in the Human Atrium
- Forschungsthema:Impact of the hERG Channel Mutation N588K on Electrical Properties in the Human Atrium
- Typ:Studienarbeit
- Betreuung:
- Bearbeitung:
Projekt
Vorhofflimmern ist die häufigste Form anhaltender Herzrhythmusstörungen und geht mit einer Zunahme der Mortalität und einem erhöhten Schlaganfallrisiko einher. Häufige Ursachen von Vorhofflimmern sind strukturelle Herzerkrankungen. In ungefähr 10% der Fälle kann jedoch keine zu Grunde liegende strukturelle Herzerkrankung nachgewiesen werden. Als Ursache dieser Formen werden genetische Defekte angenommen. Einige Vorhofflimmer-Syndrome sind bekannt. Eines davon ist die Mutation N588K im Gen KCNH2. KCNH2 kodiert das Protein hERG, welches die alpha-Untereinheit des schnellen verzögerten Kaliumkanals bildet (IKr-Kanal).
Die an der Entstehung von Vorhofflimmern beteiligten Prozesse sind komplex und bislang nur unvollständig verstanden. Erkenntnisse über genetisch bedingte Veränderungen tragen dazu bei, grundlegende Mechanismen in der Entstehung von Vorhofflimmern zu verstehen. Mit Hilfe elektrophysiologischer Messtechniken lassen sich die Veränderungen der betroffenen Ionenkanälen bestimmen. Durch Integration dieser Daten in Computer-Modelle des Herzens ist eine Untersuchung der Entstehung von Herzrhythmusstörungen möglich.
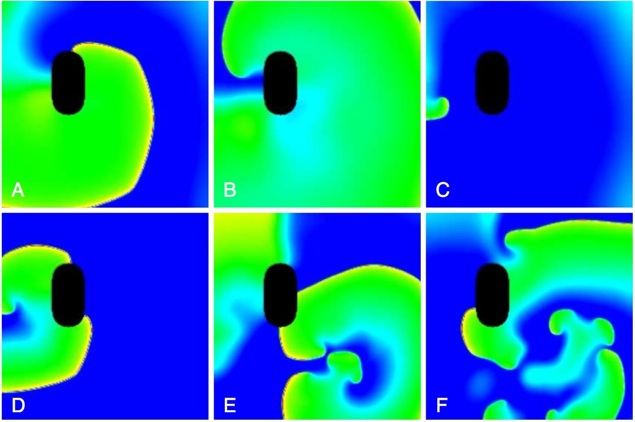
In dieser Studienarbeit wird der Einfluss der Kanalmutation N588K im Computermodell untersucht. Dazu erhalten wir aus der Arbeitsgruppe „Molekulare Elektrophysiologie“ der Universität Heidelberg Messdaten des gesunden und des mutierten Kanals (whole cell voltage clamp). Diese werden mit Hilfe von Optimierungstechniken so in das Modell integriert, dass der Unterschied der Eigenschaften von Messung und Modell minimal sind. Das Modell des Kanals wird dann in ein menschliches Vorhofmodell integriert. Zunächst werden die Eigenschaften der Zelle bestimmt, um danach den Einfluss auf die Erregungsausbreitung und um die Repolarisation zu charakterisieren. Schließlich wird das Modell in ein vereinfachtes zwei-dimensionale Modell bzw. ein realistisches Modell des menschlichen Vorhofs integriert. In beiden Geometrien sollen die Eigenschaften von Flattern und Flimmern für die spezifische Mutation untersucht werden. Zusätzlich wird eine Stabilitätsanalyse durchgeführt, die zeigen soll, bei welchen Randbedingungen die Wahrscheinlichkeit für Arrhythmien groß ist.

